Produk IVD adalah perangkat dan sistem yang digunakan untuk mendiagnosis, mengobati, atau mencegah kondisi kesehatan. Mereka dimaksudkan untuk digunakan dalam pengumpulan dan pemeriksaan sampel biologis seperti darah, air liur, atau jaringan. Sampel dapat diambil dari dalam hidung atau bagian belakang tenggorokan, atau dari vena atau ujung jari.
Penting untuk dicatat bahwa produk IVD tidak invasif. Misalnya,
penganalisis imunoassay chemiluminescence homogen Poclight HSCL-5000 Mikro
.
Namun, mereka masih dianggap sebagai perangkat medis dan oleh karena itu tunduk pada kontrol yang sama. Alat kesehatan terdiri dari setiap instrumen, alat, perangkat lunak, atau perangkat terkait yang dimaksudkan untuk digunakan bagi manusia untuk tujuan:
·
Mendiagnosis, mencegah, memantau, atau mengobati penyakit atau cedera.
·
Mendukung atau menopang kehidupan.
·
Mengatur konsepsi.
·
Desinfeksi alat kesehatan.
·
Memberikan informasi untuk tujuan medis dengan mengumpulkan sampel biologis dari manusia.
Produsen Diagnostik In Vitro harus memenuhi persyaratan peraturan Uni Eropa, Inggris Raya, dan AS tergantung pada pasar yang ingin mereka tembus.
Persyaratan ini termasuk Peraturan Diagnostik In Vitro (IVDR) (EU) 2017/746 di UE dan Peraturan Perangkat Medis Inggris (UK MDR) 2002 di Inggris. Di Amerika Serikat, produk IVD didefinisikan dalam pasal 201(h) Federal Food, Drug, and Cosmetic Act (FD&C Act); perangkat ini juga dapat tunduk pada pasal 351 Undang-Undang Layanan Kesehatan Masyarakat, serta kategorisasi di bawah Amandemen Peningkatan Laboratorium Klinis (CLIA) tahun 1988.
Menurut IVDR, produk IVD didefinisikan sebagai “setiap perangkat medis yang merupakan reagen, produk reagen, kalibrator, bahan kontrol, kit, instrumen, aparatus, bagian dari peralatan, perangkat lunak atau sistem, baik digunakan sendiri atau dalam kombinasi, dimaksudkan oleh pembuatnya untuk digunakan secara in vitro untuk pemeriksaan spesimen, termasuk donor darah dan jaringan, yang berasal dari tubuh manusia…”
Para ahli memperkirakan bahwa sekitar 70% dari semua keputusan klinis dibuat dengan menggunakan produk IVD.
Contoh Produk IVD
Tes kehamilan, tes COVID-19, dan tes HIV adalah contoh produk IVD. Contoh lain perangkat Poclight HSCL-5000 Micro CLIA Analyzer IVD meliputi:
·
Diagnostik kanker
· Diagnosis tiroid
· Diagnosis peradangan
·
Imunoassay
· ...
Wadah yang diproduksi untuk spesimen medis juga merupakan produk IVD. Menurut Organisasi Kesehatan Dunia, lebih dari 40.000 produk tersedia untuk pengujian IVD hari ini. Ini dapat berkisar dari tes laboratorium tradisional hingga tes di tempat perawatan.
Klasifikasi IVD
Di Amerika Serikat, FDA mengklasifikasikan semua perangkat medis—termasuk produk IVD—sebagai Kelas I, Kelas II, atau Kelas III. Klasifikasi perangkat akan bervariasi berdasarkan risiko yang terlibat dan tingkat kontrol regulasi yang diperlukan untuk menjamin keamanan produk. Dengan demikian, klasifikasi IVD akan menentukan proses pra-pemasaran yang harus diikuti oleh produsen untuk membawa produk mereka ke pasar.
·
Produk Kelas I dianggap berisiko rendah hingga sedang dan memerlukan pengendalian umum.
·
Produk Kelas II dianggap berisiko sedang hingga tinggi dan memerlukan pengendalian umum dan Pengendalian Khusus.
·
Produk Kelas III dianggap berisiko tinggi dan memerlukan kontrol umum dan Premarket Approval (PMA).
Penting untuk dicatat bahwa saat kelas perangkat meningkat, kontrol regulasi juga meningkat. Perangkat IVR Kelas I tunduk pada kontrol regulasi paling sedikit, sedangkan perangkat IVR Kelas III memiliki persyaratan yang paling ketat. Perusahaan Life Sciences yang ingin membawa produk Diagnostik In Vitro mereka ke pasar di Amerika Serikat dapat merujuk ke sumber daya "Klasifikasi Perangkat Medis Anda" FDA.
Ingin memastikan kepatuhan terhadap peraturan di Uni Eropa? IVDR ditingkatkan pada tahun 2021 untuk mencakup peningkatan seperti:
·
Kewajiban yang jelas bagi produsen, importir, dan distributor yang melibatkan ketertelusuran perangkat, pendaftaran, dan verifikasi pelabelan yang tepat. Ini termasuk sistem keterlacakan yang didasarkan pada pengenal perangkat unik (UDI).
·
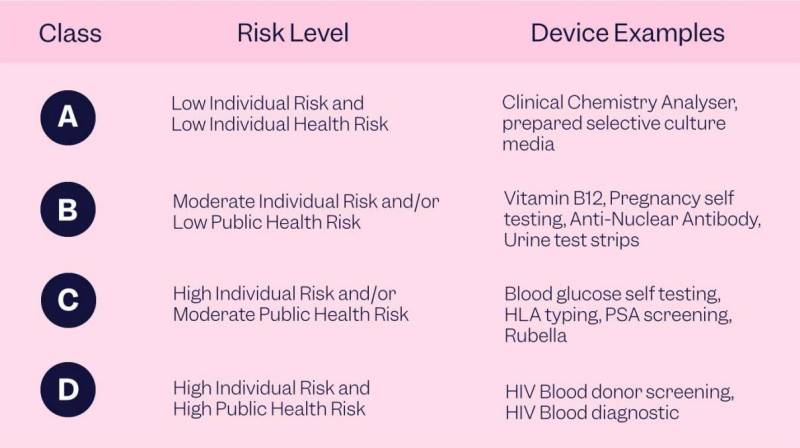
Pengenalan klasifikasi yang terdiri dari empat kelas risiko. Perangkat Kelas A memiliki risiko kesehatan individu dan masyarakat yang rendah, perangkat Kelas B memiliki risiko kesehatan individu dan/atau masyarakat yang rendah, Perangkat Kelas C memiliki risiko individu tinggi dan/atau risiko kesehatan masyarakat sedang, dan perangkat Kelas D memiliki risiko individu tinggi dan tinggi risiko kesehatan masyarakat.
·
Kontrol yang lebih ketat untuk perangkat IVD berisiko tinggi.
·
Pengawasan yang terjamin dari badan yang diberitahukan (atau badan penilaian kesesuaian pihak ketiga yang independen) dengan memperkuat serangkaian kriteria tertentu.
·
Transparansi yang lebih besar dengan database yang komprehensif pada perangkat medis di UE (disebut EUDAMED).
·
Memperkuat bukti klinis dan peraturan evaluasi kinerja, dengan lebih banyak koordinasi di antara negara-negara UE—terutama terkait pengawasan pasar.
·
Persyaratan pengawasan pasca-pasar produsen yang lebih kuat.
·
Persyaratan khusus untuk “perangkat internal”, atau produk IVD yang diproduksi dan digunakan dalam institusi yang sama.
Membawa produk IVD ke pasar dengan aman dan efektif adalah kuncinya—dan memahami peraturan yang berlaku adalah langkah pertama yang ideal.
Kesimpulan
Produk IVD adalah garis pertahanan kritis terhadap berbagai kondisi kesehatan. Keamanan dan kualitas Diagnostik In Vitro sangat penting, itulah mengapa kepatuhan terhadap peraturan pabrikan sangat penting. Poclight bersertifikat CE dan ISO dan memiliki rangkaian lengkap item reagen untuk membuat pengujian tanpa khawatir.

 English
English français
français русский
русский español
español português
português العربية
العربية 日本語
日本語 Türkçe
Türkçe हिंदी
हिंदी Indonesia
Indonesia 







 Jaringan IPv6 didukung |
Jaringan IPv6 didukung | 